Es una condición que afecta las habilidades cognitivas y se estima que en 2030 podría alcanzar a unas 7 millones de personas en todo el mundo. Qué causa esta demencia.
 Es importante considerar tanto los factores putativos protectivos (que tienen un efecto protector o mitigador) así como los factores de riesgo en la EA (Imagen ilustrativa Infobae)
Es importante considerar tanto los factores putativos protectivos (que tienen un efecto protector o mitigador) así como los factores de riesgo en la EA (Imagen ilustrativa Infobae)Recientemente el Instituto Nacional de la Asociación del Envejecimiento y la EA la ha caracterizado operacionalmente como una construcción biológica constituida por la presencia en el cerebro de placas compuestas por una proteína anormal (βamiloide), ovillos tau y neurodegeneración irrespectivamente de la expresión clínica.
La cascada de eventos fisiopatológicos comienza 20 a 30 años antes que se manifieste clínicamente. Es decir, la EA puede ser diagnosticada antes de que se desarrolle la demencia en individuos con trastornos mínimos de la cognición, declinación cognitiva subjetiva o cognición normal.
La tau derivada del cerebro y la βamiloide pueden actualmente ser evaluadas en suero, debido a que se ha encontrado que los valores séricos son concordantes con los hallados en líquido cefalorraquídeo (LCR), y a través de los marcadores por neuroimágenes tales como la Resonancia Magnética (RM) y la Tomografía por emisión de Positrones (PET).
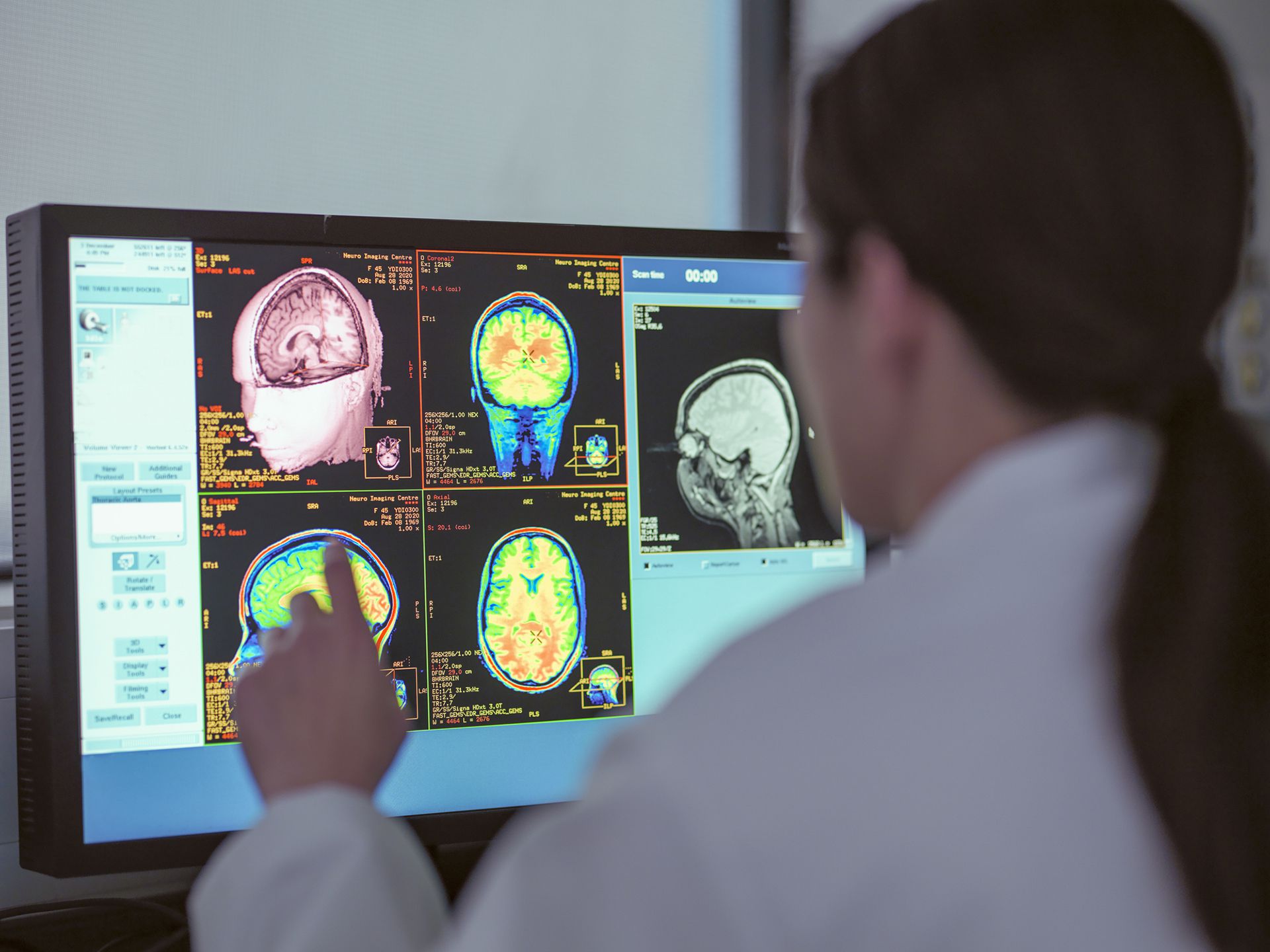 Formación médica adecuada para identificar pacientes con trastorno cognitivo leve y demencia leve de tipo Alzheimer (Getty)
Formación médica adecuada para identificar pacientes con trastorno cognitivo leve y demencia leve de tipo Alzheimer (Getty)
En la RM se observa predominantemente atrofia de la región temporal medial y en el PET disminución del metabolismo parietal y temporal. Además, en PET es posible distinguir pacientes con EA de controles normales cuando se utilizan isótopos para visualizar las placas amiloideas.
Por otro lado, los factores de riesgo incluyen ciertos genes tales como la apolipoproteina APOE 4, la edad, historia familiar, traumatismos de cráneo y aislamiento social, así como todos aquellos asociados con ateroesclerosis (hipercolesterolemia, diabetes, hipertensión arterial, tabaquismo, obesidad, etc.).
El tratamiento farmacológico hasta hace muy poco tiempo ha sido exclusivamente sintomático basado en drogas que mejoran el déficit colinérgico (inhibidores de la colinesterasa) y por ende la memoria; la mejoría clínica puede mantenerse hasta 2 años. También la memantina puede producir mejoría en los síntomas conductuales y en cierta forma también en la autonomía.
 La enfermedad de Alzheimer (EA) es responsable del 60% al 70% de los casos. En América Latina y el Caribe vivían con demencia en 2010 alrededor de 3 millones a 4 millones de personas
La enfermedad de Alzheimer (EA) es responsable del 60% al 70% de los casos. En América Latina y el Caribe vivían con demencia en 2010 alrededor de 3 millones a 4 millones de personas
Actualmente la aprobación en Estados Unidos de dos anticuerpos monoclonales lecanemab y aducanumab, mientras hay muchos más en estudio, y su incorporación en la práctica clínica han redefinido el tratamiento de la EA. Diversos estudios han demostrado que disminuyen los depósitos de amiloide cerebral y enlentecen la progresión del deterioro cognitivo en alrededor de un 25% por año. Es probable que el beneficio sea acumulativo cuando se realiza el tratamiento a largo plazo.
Sin embargo, el tratamiento con anticuerpos monoclonales requiere varias consideraciones para que sea tanto efectivo como seguro.
A saber:
1-Formación médica adecuada para identificar pacientes con trastorno cognitivo leve y demencia leve de tipo Alzheimer
2-Requerimiento de nuevos recursos en la práctica clínica, tales como la evaluación de biomarcadores en suero o LCR y dosaje de APOE así como personal entrenado para evaluar los depósitos de amiloide en PET y las anormalidades en RM
3-Accesibilidad y personal entrenado para la infusión endovenosa de las drogas
4-Médicos capacitados para reconocer, diagnosticar y eventualmente tratar las complicaciones del tratamiento. Estas consisten en reacciones adversas a la infusión y particularmente en la aparición de anormalidades en la RM (por ejemplo edema, hemorragias) que pueden ocasionalmente producir déficits neurológicos
5-Los costos de los anticuerpos monoclonales son todavía muy elevados.
 Se requiere de nuevos recursos en la práctica clínica, tales como la evaluación de biomarcadores en suero o LCR y dosaje de APOE así como personal entrenado para evaluar los depósitos de amiloide en PET y las anormalidades en RM (Getty)
Se requiere de nuevos recursos en la práctica clínica, tales como la evaluación de biomarcadores en suero o LCR y dosaje de APOE así como personal entrenado para evaluar los depósitos de amiloide en PET y las anormalidades en RM (Getty)
La terapéutica antiamiloidea ha abierto una nueva era en nuestro desafío de proteger el cerebro humano, aunque por si sola no es suficiente. Las investigaciones actuales están dirigidas a la combinación de drogas, vacunas, terapia génica y antiinflamatoria e inclusive la estimulación magnética transcraneal.
En estudio existen diversas vacunas anti-tau y anti-amiloide para estimular los mecanismos de defensa cerebral de forma tal que reconozcan y destruyan las proteínas anormales. La terapia génica también está en estudio; la inyección del gen APOE 2, que es beneficioso y disminuye el riesgo de la enfermedad, puede mitigar los efectos negativos del gen APOE4.
Nuestra sociedad valora la salud y la dignidad de las personas mayores, quienes merecen acceso a los mejores y más avanzados tratamientos posibles. Los progresos científicos deben integrarse al sistema de salud a través de mecanismos sociales y políticos que posibiliten la disponibilidad para los pacientes con necesidades urgentes.
La incorporación de los anticuerpos monoclonales a la práctica clínica han redefinido el tratamiento de la enfermedad de Alzheimer debido a que enlentecen la progresión del deterioro cognitivo. Más aún, las investigaciones actuales están dirigidas a la combinación de drogas, vacunas, terapia génica con G y antiinflamatorios, entre otros, con los cuales se obtendrá un mayor beneficio terapéutico.
*Ramón Leiguarda es profesor Consulto de Neurología (UBA). Miembro de la Academia Nacional de Medicina




